氮气的临界压缩系数
氮气在标准状况下的临界压缩因子为0.2 9 2 ,其分子式为N2 ,它通常以无色无味的气态存在,普遍认为是无害的,且其密度低于空气。大气中氮气的体积占比约为7 8 .1 2 %,是构成空气的主要成分。
在标准大气压力下,氮气在冷却至-1 9 5 .8 ℃时会转变为无色液体,继续冷却至-2 09 .8 ℃时,液态氮将转变为类似雪的固态。
氮气化学性质相对稳定,在常温下难以与其他物质发生反应,但在高温或高能量环境下,它能与某些物质发生化学反应,用于合成对人类有益的新化合物。
氮气在常温常压下保持无色无味,无毒,其体积分数占大气7 8 .1 2 %,在标准状况下密度为1 .2 5 g/L,且不易溶于水,在常温常压下,水中的氮气溶解度约为每升水中溶解0.02 体积的氮气。
氮气不易液化,在极低温度下可液化成无色液体,进一步降温则形成白色晶体固体。
工业上,氮气通常存储在黑色钢制气瓶中。
详细的物理性质请参考下表。
空气的压缩系数
压缩因子(Compre ssibility Factor),有时也称作气体压缩系数(Compre ssibility Coefficient),它反映了真实气体行为与理想气体理论的偏差程度。这个系数通常用字母Z来表示,其计算公式为Z = Pv/RT,也可以写成Z = Pvm/RuT。
这里的P代表气体的绝对压力,vm是气体的摩尔体积,Ru是通用气体常数,R是气体的摩尔气体常数,而T则是热力学温度。
Z的值越远离1 ,意味着实际气体的行为越偏离理想气体。
压缩因子Z在描述实际气体的状态方程中扮演着重要角色。
特别是在计算气体流量时,考虑到Z是必不可少的。
通常,当气体的压力不是特别高,温度相对较高,且密度较小时,使用理想气体状态方程来计算就足够满足一般工程需求,此时Z的值等于1 然而,在高压、低温或需要高精度计算的情况下,就必须采用实际气体状态方程,并考虑压缩系数。
特别是在计量气体流量时,由于对计算精度要求较高,压缩系数几乎总是需要被纳入考量。
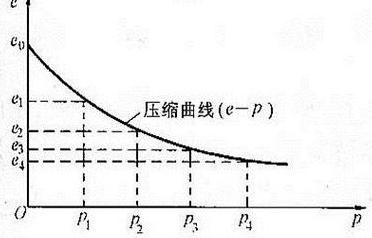
值得注意的是,空气的压缩系数会随着温度和压力的变化而变化,具体数值如图表所示。